{RANDOM_PARAGRAPH=100-400}
Защита корпуса судна от коррозии
Из различных видов коррозии в морских условиях основной является электрохимическая — разрушение поверхности металла в жидкостях, проводящих электрический ток (электролитах) . Если в электролит поместить соединенные между собой электроды — металлы, имеющие разный потенциал, то электрод с более низким значением потенциала (анод) будет разрушаться, а по проводнику, соединяющему электроды, будет проходить электрический ток.
В судовых условиях электролитом является морская вода, а роль электродов выполняют стальной корпус и бронзовые втулки в дейдвудной трубе и рулевых петлях, а также бронзовый или латунный гребной винт. Медь и ее сплавы, обладая более высоким потенциалом, при контакте со сталью создают катод. В результате этого сталь, являющаяся анодом, подвергается значительному коррозионному разрушению, особенно на участках, близко расположенных к контакту. При отсутствии разнородных металлов гальванические пары образуют сталь с прокатной окалиной, которая имеет потенциал более положительный, чем потенциал железа, поэтому она по отношению к местам, не имеющим окалины, играет роль катода. Это вызывает бурный процесс электрохимического разрушения анодных участков. Подобным же образом действуют различные примеси и шлаковые включения, содержащиеся в стали, а также окрашенные участки.

Борьба с коррозией проводится различными способами. Но все они являются разновидностью одного из следующих методов: легирование, ингибиторная защита, защитные покрытия и электрохимическая защита.
Выбор способа защиты зависит от назначения конструкции и условий ее эксплуатации.
Легирование. Для повышения коррозионной стойкости стали в качестве легирующих элементов применяют хром, никель, титан, молибден и некоторые другие элементы. Но достаточная эффективность нержавеющей стали в морской воде обеспечивается только при содержании в ней легирующих элементов свыше 18 %, что значительно повышает стоимость стали. Поэтому легирование не нашло широкого распространения в судостроении. Из нержавеющей стали изготовляют только винты и подводные крылья, а в судовом машиностроении она используется в качестве заменителя цветных металлов.
Ингибиторная защита. Ингибиторами, или замедлителями коррозии, называют такие вещества, которые при добавлении в небольших количествах к агрессивной среде замедляют или предупреждают коррозию.
Ингибиторную защиту применяют только в закрытых помещениях. Поэтому этот вид защиты может найти применение главным образом на нефтеналивных судах для предупреждения коррозии внутренних поверхностей грузовых танков. В этом случае ингибиторы могут вводиться как в нефтепродукты, так и в принимаемую балластную воду. Общее количество вводимого при этом замедлителя обычно составляет несколько сотых процента. Обычно замедлитель вводят в раствор, которым промывают танки после удаления груза или балласта.
Защитные покрытия. Наиболее простая защита от коррозии — это нанесение на поверхность металла защитной пленки. В зависимости от вида защитной пленки Покрытия бывают лакокрасочные, металлические, неметаллические и оксидные.
Лакокрасочные покрытия наиболее широко применяют в судостроении. Этому способствуют сравнительно низкая их стоимость и простота выполнения, а также вполне удовлетворительная эффективность в случае качественного выполнения всех подготовительных и окрасочных работ. Нанесенные тонким слоем на поверхность, лакокрасочные покрытия после высыхания превращаются в плотную эластичную пленку, которая не только отделяет металл от внешней среды, но и препятствует образованию гальванических пар на поверхности металла.
Металлические покрытия применяют значительно реже. В качестве покрытий могут применяться различные металлы (медь, цинк, олово, никель, хром и др.). В судостроении наиболее широко используется цинкование, которому подвергаются большинство трубопроводов судовых систем и некоторые дельные вещи. Цинковое покрытие, имея хорошее сцепление с основным металлом, обладает сравнительно низкой механической прочностью. Поэтому его необходимо оберегать от ударов твердыми и острыми предметами, которые могут вызывать местные повреждения и царапины защитного слоя.

Неметаллические покрытия имеют низкую стоимость. Во многих случаях их применение дает значительную экономию средств. Отсеки двойного дна и пики обычно покрывают водным раствором цемента, а малодоступные места заливают бетоном. Цемент и бетон наиболее целесообразно использовать также для покрытия льял, ватервейсов и других мест, где скапливается вода.
На судах, перевозящих грузы, способствующие коррозионному разрушению, можно производить битумирование внутренних поверхностей грузовых трюмов. Нанесение битумного покрытия требует предварительной грунтовки поверхности смесью нефтяного битума с бензином. Покрытие наносят на защищаемую поверхность вручную или специальным насосом. Перед нанесением битум или мастику нагревают до температуры около 200 “С.
Широкое внедрение в народное хозяйство пластмассовых материалов позволяет значительно расширить номенклатуру и область применения неметаллических покрытий. К таким покрытиям относится, например, защитный материал типа «Нева».
Защита металлических судов от коррозии и обрастания с помощью лакокрасочных покрытий
Защита от коррозии. Для предупреждения любого коррозионного процесса можно использовать следующие основные способы:
устранить причину коррозии (контакт с электролитом);
применить пассивную защиту, затрудняющую возникновение и развитие коррозионных процессов, но не устраняющую их причины (окрашивание);
использовать активную защиту, которая заключается в воздействии на причину коррозии (катодная защита, при которой устанавливается режим, снижающий разрушение корпуса судна);
использовать анодную защиту.
В судостроении применяют три последних способа борьбы с коррозией, так как исключить контакт корпуса судна с электролитом (морской водой) невозможно.
Пассивная защита может быть осуществлена путем нанесения на корпус судна, корпусную конструкцию или изделие защитного покрытия: металлического, органического или неорганического. Металлические покрытия могут быть анодными или катодными. Цинковые покрытия, относящиеся к анодным, не только изолируют металл от влияния внешней среды, но и защищают его электрохимически. К органическим покрытиям относятся жидкие, пастообразные, без растворителей или порошковые лакокрасочные материалы. Неорганические защитные покрытия получаются в результате химической обработки металла. Вследствие значительной пористости сами по себе окисные или фосфатные пленки не могут служить надежным защитным покрытием для металла. Такие пленки только улучшают адгезию лакокрасочного покрытия с окрашиваемой поверхностью, что повышает противокоррозионную защиту металла.
В основе активной защиты лежат электрохимические способы борьбы с коррозионными процессами. При катодном способе защиты корпус судна присоединяется к постороннему источнику постоянного тока, и он служит катодом. В качестве анодов используют дополнительные электроды, специально устанавливаемые на внешней поверхности корпуса, которые при этом разрушаются.
Анодная, или протекторная, защита заключается в следующем: к защищаемой конструкции присоединяют пластину металла, менее благородного, чем защищаемый металл, т. е. имеющего более низкий электродный потенциал. Такая пластина (протектор) становится анодом, на котором искусственно сосредоточивается коррозия. Разрушенный протектор заменяют новым. В судостроении применяют протекторы из цинка, алюминия, магния, сплавов алюминия с цинком, магния с алюминием, цинком и т. п. Наиболее эффективна протекторная защита в сочетании с лакокрасочными покрытиями.
Для защиты от коррозии наиболее часто используют лакокрасочные покрытия, которые по сравнению с другими видами защитных покрытий, служащих для тех же целей, имеют следующие преимущества:
низкую стоимость (по сравнению, например, со стоимостью гальванических, порошковых, стеклоэмалевых и других покрытий);
высокую технологичность (нанесение красок менее сложно, чем нанесение других видов защитных покрытий; окрашивать можно изделия любой конфигурации и размера, полностью или частично);
длительный период действия при правильном выборе лакокрасочных материалов, технологии их нанесения и схемы окрашивания;
возможность быстрого возобновления покрытия в случае его повреждения или разрушения, даже на эксплуатируемом судне.
Кроме того, путем соответствующего подбора красок и технологии их нанесения можно получить покрытия, обладающие практически любыми требуемыми свойствами (негорючие, теплостойкие, нефтестойкие, кислотостойкие, нескользкие, противообрастающие, химически стойкие и т. п.), а также любого заданного цвета и желаемой фактуры (глянцевые, матовые, полуматовые, шероховатые и др.).
Выбирая способ защиты, необходимо учитывать условия, в которых будет находиться изделие при эксплуатации. Поэтому для окрашивания судов следует применять покрытия, обладающие хорошей водостойкостью, твердостью и износоустойчивостью.
Для длительной защиты изделия от действия внешней среды необходимо, чтобы пленка покрытия была сплошной, лишенной пор, сохраняла высокую адгезию к поверхности, обладала минимальным водопоглощением. На практике при многослойном окрашивании не удается полностью изолировать окрашиваемую поверхность от действия влаги и кислорода воздуха вследствие неизбежного наличия в пленке краски пор, способности ее к набуханию, постепенного проникновения влаги к металлу и ухудшения адгезии покрытия к окрашенной поверхности. Особенно опасны разрушения краски в тех случаях, когда на поверхности стали 1 имеются остатки окалины, неизбежно создающие на металле анодные 2 и катодные 3 участки (рис. 2.3).

Рис. 2.3. Возникновение коррозионных процессов при наличии на металле окалины: а — на стальном листе с остатками окалины имеются анодные и катодные участки; б — сплошная пленка лакокрасочного покрытия защищает анодные участки от разрушения; в — при повреждении лакокрасочного покрытия на анодных участках возникает коррозия; г — нанесение протекторной грунтовки усиливает защиту анодных участков; д — повреждение краски вызывает разрушение только протекторной грунтовки.
При нанесении защитного покрытия 4, изолирующего металл, коррозионные процессы прекращаются. Однако по мере набухания покрытия, сопровождающегося его повреждением немедленно начинается коррозия металла, приводящая к появлению в анодных зонах глубоких местных разрушений. Неблагоприятное влияние остатков окалины или ржавчины можно ослабить применением протекторной грунтовки 5, которую затем перекрывают противокоррозионной краской.
Для того чтобы надежно защитить окрашиваемую поверхность, необходимо применять краски, в состав которых входят пигменты, способные замедлять коррозию металла. Это свойство пигментов называется ингибирующей способностью.
Все пигменты, используемые для изготовления красок, могут быть разделены на инертные (алюминиевая пудра, титановые белила, хромовый желтый пигмент и др.), замедляющие коррозию (свинцовый и цинковый крон, свинцовый сурик, цинковая пыль и др.) и способствующие коррозии (мумия, сажа, железный сурик из пиритных огарков и др.).
Замедляющее влияние на коррозию красок, в том числе содержащих алюминиевую пудру, не всегда можно объяснить только электрохимической протекторной защитой. Высокие противокоррозионные свойства таких красок в значительной степени зависят от их малой набухаемости и проницаемости вследствие чешуйчатого строения частиц алюминиевой пудры.
Свинцовый крон к числу универсальных замедлителей коррозии не относится. Цинковый крон является одним из универсальных замедлителей коррозии для стали и легких сплавов, но только в нейтральной или щелочной среде. В кислой среде, наоборот, он усиливает коррозию.
Наблюдениями установлено, что лакокрасочные покрытия, содержащие в своем составе пигменты, являющиеся замедлителями коррозии, оказывают защитное действие на окрашенную металлическую поверхность даже после повреждения покрытия.
Большое значение имеет технология получения лакокрасочных покрытий. Основные требования, от выполнения которых зависит качество покрытия, заключаются в следующем:
окрашиваемые поверхности должны быть сухими и полностью очищенными от всяких загрязнений;
окрашивание нужно производить рекомендованными материалами в сухую погоду при температуре и относительной влажности воздуха, установленных для покрытия;
количество нанесенных слоев и общая толщина высохшего слоя покрытия должны отвечать заданным;
окрашивание необходимо выполнять способами, указанными в технологии, с помощью рекомендованного оборудования и инструментов;
эксплуатация окрашенного судна должна быть начата только после полного высыхания всех нанесенных слоев краски.
Очень важно очистку металла выполнять так, чтобы на его поверхности не появлялись выступы и глубокие впадины, поскольку на выступающие участки практически невозможно нанести слой краски нужной толщины. При эксплуатации в этих точках происходит быстрое разрушение покрытия и появляется значительное количество очагов коррозии, устранить которые можно только нанесением дополнительных слоев красок. Впадины тоже способствуют быстрому разрушению защитного покрытия. Скапливающаяся в них краска до начала эксплуатации не успевает достаточно хорошо просохнуть. При попадании в воду полувысохшая краска на этих участках набухает и быстро разрушается.
аноды на прогресс
"Справочник по катерам,лодкам и моторам".Под общей редакцией Г.М.Новака.Стр.324-327.
#4 motoras
- Из: Дзержинск
- Судно: Адмиралец
- Название: АЛАГАЗ
просил же ДЕЛЬНЫЙ совет. то о чем пишут в таких кнмгах уже давно не выпускают. интересует где можно найти(купить) в наши дни или сделать из чего(советовать сделать из куска цинка не нужно) конкретно.
Сообщение отредактировал motoras: 04 мая 2010 – 08:23
#5 валенок
- Из: Речновск
просил же ДЕЛЬНЫЙ совет. то о чем пишут в таких кнмгах уже давно не выпускают. интересует где можно найти(купить) в наши дни или сделать из чего(советовать сделать из куска цинка не нужно) конкретно.
#6 motoras
- Из: Дзержинск
- Судно: Адмиралец
- Название: АЛАГАЗ
Сделать из чего аноды?Курс химии средней школы,а конкретно-электрические потенциалы и ряд активности металлов по отношению к водороду.
Ну ты загнул. Человек спросил конкретно. Чего и откуда нужно отломать что бы со смыслом прикрутить на Прогресс. У людей и так голова забита решением жизненных проблем. А ты его в среднюю школу посылаешь, которая была давно и не правда.
Про батарейки. Нужно постараться найти в бумажной изоляции. А то современные жестяные неудобны в разборке. Хотя при переплавке цинк должен легко отделиться. Есть еще военные батареи. Вот с них цинку по больше будет. И еще. Важна не толщина, а площадь поверхности.
Сообщение отредактировал motoras: 04 мая 2010 – 09:21
#7 валенок
- Из: Речновск
Ну ты загнул. Человек спросил конкретно. Чего и откуда нужно отломать что бы со смыслом прикрутить на Прогресс. У людей и так голова забита решением жизненных проблем. А ты его в среднюю школу посылаешь, которая была давно и не правда.
Про батарейки. Нужно постараться найти в бумажной изоляции. А то современные жестяные неудобны в разборке. Хотя при переплавке цинк должен легко отделиться. Есть еще военные батареи. Вот с них цинку по больше будет. И еще. Важна не толщина, а площадь поверхности.
Сообщение отредактировал валенок: 04 мая 2010 – 09:34
#8 StrangerM
- Из: СПб
- Судно: МН
- Название: Stranger
появилась коррозия на килевой накладке на п2 в виде точек белого порошка. как бороться вроде понятно. хочу поставить аноды. какие, где взять?много написано про аноды для котлов отпления но одни общие фразы. просьба не посылать в поиск(был). кто может дать дельный совет?
Сообщение отредактировал StrangerM: 04 мая 2010 – 09:32
#9 гоша5
- Из: тольятти
- Судно: прогресс 2
Сделать из чего аноды?Курс химии средней школы,а конкретно-электрические потенциалы и ряд активности металлов по отношению к водороду.
эх валенок валенок! если ты про это
то это я знаю. в теории мы все сильны. я спрашиваю ГДЕ на практике можно добыть или из ЧЕГО можно сделать аноды магниевые или цинковые (например : берем то-то пилим попалам. и т.д.) нужен ДЕЛЬНЫЙ совет просто так по клаве хлопать не стоит.
#10 валенок
- Из: Речновск
эх валенок валенок! если ты про это

то это я знаю. в теории мы все сильны. я спрашиваю ГДЕ на практике можно добыть или из ЧЕГО можно сделать аноды магниевые или цинковые (например : берем то-то пилим попалам. и т.д.) нужен ДЕЛЬНЫЙ совет просто так по клаве хлопать не стоит.
#11 StrangerM
- Из: СПб
- Судно: МН
- Название: Stranger
#12 гоша5
- Из: тольятти
- Судно: прогресс 2
Ну, это практика. А позвольте узнать – куда и как вы будите крепить протекторы?
#13 StrangerM
- Из: СПб
- Судно: МН
- Название: Stranger
крепить на место крепления колес через прокладку из диэлектрика.
#14 гоша5
- Из: тольятти
- Судно: прогресс 2
Для правильной работы протектора необходимо, чтобы он имел надежный электрический контакт с защищаемой поверхностью. Ведь ток электрокоррозии течет, для примера, следующим образом. АМГ корпус – вода(электролит) -стальной вал – контакт – АМГ корпус. Задача защиты обеспечить отвод тока на протектор. А именно АМГ корпус – протектор – вода(электролит) – стальной вал – контакт – АМГ корпус- протектор. При этом часть тока будет течь по старому контуру, эта часть зависит от площади протектора и его расположения на АМГ корпусе относительно стального вала. Повторяю, это пример. Из примера следует, что важно найти "стальной вал", т.е. второго участника пары. Если разорвать электрический контур в любом месте, то ток перестанет течь, тогда и протоктор может стать ненужным.
АНОД-обоснование его необходимости (Просматривает: 1)

Извините, речь от этом идет (см. фото) 
sollo7
Seppoman
Апнем темку.
Мотор стал покрываться "жуками". Лакокрасочное покрытие пузырится и под ним белый налет. Мотор эксплуатируется на финском заливе. Может быть, что анод не работает?
Sleepy_PIP
а сколько времени мотор у Вас в воде? и какой? если равно моточасам – то в общем-то не стоит задумываться, но и ничего снимать не надо .
Но вот если у вас мотор в воде все время пока она жидкая – то защита хорошо побережет мотор даже в пресной воде.
Кстати и для металл. корпусов существуют и разумеется применяются электрохим защиты. пассивные и активные.
Африканыч
А на мои аноды воду нельзя, ипанёт,почти 3000 вольт
Мне такой необходим.
Вложения
Проектор
Мётчик
Amurru
Дмитрий Е
Мётчик
@leksei
Real Gek
Учитывая то, что проблемы коррозии – сфера моих професиональных компетенций, решил раскрыть тему. Коротко о себе. Профильная специальность в институте, более 30 лет занимаюсь защитой от коррозии (10 лет в НИИ, потом в различных предприятиях), для развлечения и чтобы мозги жиром не заплывали более 20 лет преподаю электрохимическую защиту от коррозии в вузе, имею по специальности 3 патента, сколько-то (честно, не считал) статей в научных журналах, соавтор нескольких книг (3 или 4) по защите от коррозии. Ну, т.е. человек, немного в проблеме разбирающийся.
В данном тексте попробую затронуть вопросы, относящиеся только к коррозии водномоторного оборудования (особенно моторов), не вдаваясь в частности и не претендуя на строгую научность изложения. Ну и прошу извинить за занудство и многа букав.
Поехали.
Коррозия – от латинского «corrodere», что означает «разъедать».
Коррозия – самопроизвольное разрушение металлов и сплавов (почему – см. ниже) под воздействием внешних факторов окружающей среды.
Причина коррозии металлов – в их термодинамической нестабильности. Говоря простым языком – метал, добытый из руды, стремиться вернуться обратно в рудное состояние.
С водномоторной точки зрения нас интересует:
1. Коррозия исключительно металлов и сплавов (особенно алюминия).
2. Коррозия, протекающая по электрохимическому механизму (т.к. альтернативный вариант – химическая коррозия – это процесс в газах при высоких температурах без наличия воды – т.е. совсем не наш вариант).
Условия для возникновения коррозии.
Их ровно 2.
1. Наличие кислорода (из воздуха или растворенный в воде – этого более чем достаточно везде, кроме болот).
2. Наличие окружающего электролита (например воды или просто влаги). Для сведения – любая вода, кроме дистиллярованной – электролит.
Анод и катод.
Для начала коррозионного процесса необходимо возникновение макропары. Макропара чаще всего (но необязательно) возникает при прямом электрическом контакте разных металлов. Электрический ток при этом будет стекать с менее благородного металла в окружающий электролит, натекать на более благородный металл и через прямой электрический контакт между этими металлами замыкать электрическую цепь.
Металл разрушается в том месте, где ток с него стекает в окружающий электролит. Это место называется анод.
Металл защищается в том месте, где ток натекает на него из окружающего электролита. Это место называется катод.
Причем, чем более разнородны металлы (см. ниже), тем "мощнее" будет макропара, тем больше протекающий ток, тем выше скорость коррозии. Такую разнородность называют "разность электродных потенциалов" или просто "разность потенциалов".
Пример – батарейка. Пока не замкнуть контакты ток не течет, коррозионный процесс не развивается. Замкнули контакты – потек ток. Обечайка батарейки (обычно это цинк) начала разрушаться (анод). Наверное многие помнят "текущие" батарейки. Это просто коррозия оюечайки.
Термодинамическая нестабильность.
Электрохимический ряд активности металлов (наверное все помнят такой – в школьном кабинете химии около таблицы Менделева).
Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Cr→Zn→Fe→Cd→Co→Ni→Sn→Pb→H→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au
Водород – это ноль. Все что правее – благородные металлы, они при нормальных условиях не подвержены коррозии, их можно найти в природе в металлическом состоянии. Все что левее – неблагородные металлы, встречаются в природе в виде химических соединений. При контакте двух разнородных металлов корродировать будет тот из них, что расположен левее.
Пример из уроков химии: на гвоздь намотана медная проволока, это всё опущено в стакан соленой воды. К следующему уроку химии от гвоздя мало что остается (анод), а медяшка блестит как новенькая (катод).
Электрохимическая защита.
Каким образом защитить нужный нам элемент конструкции? Искусственно создать макропару, в которой наш элемент будет контакировать с менее благородным металлом. Наш металл при этом будет катодом, а менее благородный элемент анодом. Такой (менее благородный) элемент называют протектором. Разрушаясь, он защищает нужный нам элемент конструкции от коррозии.
Думаю, хватит теории. Теперь практика.
Лодочный мотор у нас состоит из разных металлов. Наиболее распространенный контакт двух металлов при этом алюминий-сталь. При этом алюминий является анодом, он и будет разрушаться если не предпринять защитных мер. Однако, здесь важны 3 момента:
1. Алюминий и сталь не сильно "разнородны". Разность потенциалов у них не большая, скорость коррозии не очень высокая в пресной воде.
2. Следствием из п.1 является то, что коррозионный процесс становится заметен только в том случае, если мотор длительное время опущен в воду.
3. В морской воде скорость коррозии будет сильно выше во-первых из за лучшей ее электропроводности по сравнению с пресной и во-вторых (это самое главное) наличия в морской воде растворенных хлорсодержащих солей (т.е. ионов хлора). Они препятствуют образованию неэлектропроводящей пассивирующейся пленки из оксида алюминия на поверхности металла.
Для защиты моторов от коррозии на них устанавливается протектор из менее благородного металла – магния, который разрушаясь, защищает металлические элекменты мотора от коррозии. Для того, чтобы протектор превратился в анод (т.е. начал работать) нужно обеспечить хороший электрический контакт между ним и мотором и погрузить протектор в электролит. В этом случае возникает электрическая цепь т.н. катодной (протекторной защиты). Анод разрушается, катод защищается.
Если же поднять мотор из воды, протектор очень быстро перестает работать анодом, т.к. электропроводящая водяная пленка стекает с мотора (мотор сохнет). Бонусом в данной ситуации является то, что по этой же причине прекращается коррозионный процесс на элементах мотора.
Я не рекомендую, это пусть производители моторов делают. Я озвучиваю техническую целесообразность:
– Если вы эксплуатируете мотор в морской воде, протектор необходим во всех случаях. Нужно тщательно следить за его работоспособностью и периодически зачищать контакт между ним и посадочным местом на моторе. Крепежный винт лучше посадить на электропроводящую (например графитовую) смазку.
– Если вы эксплуатируете мотор в пресной воде длительное время, или храните мотор в опущенном состоянии, использование протектора желательно. Думаю, для людей, читающих этот форум, т.е. априори относящихся к своей матчасти с любовью, можно посоветовать то же, что и пунктом выше. Но нужно отдавать себе отчет, что риски коррозии при ээтом сильно ниже, чем в морской воде.
– Ели вы экслуатируете мотор в пресной воде в щадящем режиме, а при стоянке мотор поднимаете из воды (например у меня 50-100 моточасов в год, дошел до места стоянки – поднял, мотор хранится в гараже) проблема коррозии для вас представляет только теоретический интерес.
Если есть вопросы – буду рад ответить.
И извиняюсь за неструктирированность,несбалансированность текста и ошибки, писал из головы, редактировать лень.
Цинк: нам пора расстаться
Мы долгие годы использовали для защиты лодочных моторов и прочих металлических деталей аноды из цинка. Но доказательств долгосрочной токсичности этого металла всё больше. Альтернативные материалы для изготовления анодов дешевле, эффективнее и безопаснее. Но почему мы продолжаем его покупать?
…Многие не задумываются о жертвенных анодах — этих любопытных «нашлёпках» из металла, которые можно увидеть на валах, рулях, корпусе и прочих скрытых под водой элементах судна. Нам известно: аноды как-то по-особенному реагируют на воду и защищают важные детали от коррозии. Мы знаем также, что со временем они разрушаются и нуждаются в замене. Всё. Казалось бы, о чём здесь еще размышлять?
Может быть, всё же подумать.
На самом деле аноды — крутые штуки. В результате естественных электрохимических реакций металлы корродируют в воде. Аноды изготовлены из сплавов с особенно привлекательным диапазоном электрохимического напряжения. Поэтому коррозионные реакции сосредотачиваются именно на элементах протекторной защиты, благополучно оставляя в покое соседние детали из металла. Это немного напоминает детский праздник, когда на стол одновременно подают торт и отварную брокколи. Сладкий десерт юные гости сразу уничтожают с аппетитом, а вот капуста остаётся нетронутой.
Такой простой подход с «подсовыванием» коррозии специальных элементов защиты одинаково хорош на совсем маленьких лодках, серьёзных яхтах, коммерческих судах и береговых сооружениях (шлюзовые ворота и доки).

Аноды-протекторы отличаются размерами, формами, методами крепления. Всё зависит от предназначения и особенностей эксплуатации.
Традиционно аноды изготавливались из цинка: настолько традиционно, что в англоязычных странах их и называют «цинки». Хотя это на самом деле эффективный материал, а для функционирования человеческого организма нужно немного соединений цинка, — в более высоких концентрациях он способен вызывать реальные проблемы. Длительное интенсивное влияние его соединений на растения, беспозвоночных, рыб воздействует как токсин. Ещё один недостаток цинковых анодов — то, что в их составе есть небольшое количество кадмия, который также может вызывать проблемы со здоровьем.
Эти данные вызывают неизбежную обеспокоенность. К примеру, южнее канадской границы, в американских штатах Калифорния и Мэрилэнд было предложено запретить использование традиционных анодов после того, как исследования выявили значительное повышение уровня содержания цинка в акваториях вблизи крупных пристаней. Так как в северной Канаде навигационный сезон короче, подобных призывов отказаться от цинка здесь не было. Однако многие считают это лишь вопросом времени: доказательств его опасности всё больше.
Альтернативы
К счастью, цинк не единственный и оптимальный выбор, когда речь идёт о защите наших лодок. Существуют нетоксичные альтернативы!
Начнём с алюминия. Такие аноды имеют многочисленные преимущества перед цинком, начиная с гораздо более высокой эффективности. Более того: превосходство алюминия над цинком как анодного материала настолько подавляющее, что он занял первое место в мире среди производителей лодочных моторов.
«Все компании, производящие двигатели для лодок и катеров, теперь устанавливают на свою продукцию аноды из алюминия», — говорит Майкл Швез, представитель канадской компании Canada Metal Pacific (CMP), выпускающей протекторную защиту. Он знает, что говорит, поскольку Canada Metal Pacific поставляет аноды практически для всех крупных производителей судовых двигателей. «Mercury, BRP, Honda, Suzuki, Yamaha, Volvo Penta — все используют алюминий. И, безусловно, это наиболее эффективный анодный материал из ныне существующих».
Главное преимущество перед привычным цинком в том, что современные алюминиевые сплавы лучше «концентрируют» коррозию на себе. Кроме того, они заметно легче и совершенно нетоксичны. И у этой медали нет другой стороны, именно поэтому защита из алюминия считается продуктом премиум-класса в сравнении с давно знакомыми цинковыми протекторами. Ирония судьбы в том, что увеличение срока службы новых анодов вызывает сомнения у пользователей: «Яхтсмены и водномоторники смотрят на анод, который разрушается медленнее, чем цинковый, и делают вывод — оно не работает!» — такое наблюдение сделал Майкл Швез. — «Видимо, мы не очень хорошо объясняли, что алюминий просто служит значительно дольше!».
Также стоит объяснять клиентам: не все алюминиевые аноды одинаковы. Лучшие сделаны из первичного металла либо отлиты из высококачественных сплавов (ранее использовавшихся, к примеру, в качестве высоковольтных линиях электропередач или как материал для прецизионного оборудования). «Одно дело — перепрофилировать сплав премиум-класса, и совсем другое — переплавка низкосортного лома», — поясняют эксперты. — «Звучит невероятно, но существуют нечестные поставщики. Они скупают на верфях использованные аноды, а потом продают их обратно судовладельцам. До следующей проверки никто ничего и не узнает, а потом начнут искать козла отпущения».
Canada Metal Pacific продает анодную защиту покупателям во всём мире, в том числе и военным. Поэтому, говорит Швез, «CMP придерживается строгой системы управления качеством ISO 9001, а наши сплавы постоянно проходят химические испытания. Именно поэтому они отвечают самым строгим техническим требованиям. Без сторонней сертификации качества как вы знаете, что получите в результате?»
Такое же внимание Canada Metal Pacific уделяет качеству магниевых анодов: это ещё более эффективный способ защиты для катеров и лодок, используемых исключительно в пресной воде. Магниевые сплавы славятся чрезвычайно активным диапазоном электрохимического напряжения: это делает их отличными «защитниками», превосходящими и цинк, и даже алюминий.
«В пресной воде никакой материал не сравнится с магнием», — отмечает Швез. — «Для морской воды мы его не рекомендуем: он слишком эффективен. Он работает так хорошо, что может исчезнуть за короткое время, и судовладелец не заметит этого. В солёной воде магний растворяется как таблетка антацида. Но вот в пресной — магниевый анод лучшее, что можно придумать».
И алюминий, и магний не только превосходят по эффективности традиционные «цинки», но ещё и дешевле. Стоимость цинка за последние 4–5 лет увеличилась вдвое. Кроме того, это тяжёлый материал, поэтому тарифы на доставку велики, да и хранить его на складе тоже непросто. Конечно, такие расходы можно было бы оправдать, будь это премиальный продукт. Но алюминий и магний — гораздо лучше и оба дешевле.
Итак, нетоксичные альтернативы работают лучше, чем цинк; дольше, чем цинк и стоят меньше, чем цинк? Почему мы продолжаем жить по-старому?
Выходя на мировой уровень
Швез отметил: хотя Canada Metal Pacific давно продаёт нетоксичные аноды, доля цинка по-прежнему составляет около 60% от общего объёма реализации. Чтобы изменить ситуацию, компания разработала новую упаковку, которая доходчивее доносит преимущества альтернативных магния и алюминия. Производители также активно работают с дистрибьюторской сетью, чтобы выйти на мировой уровень.
«Мы должны дать людям понять: для цинка есть замена, которая служит лучше и стоит меньше», — говорит Швец. — «Сегодня яхтсмен в отделе запчастей просит «новые цинки» и покупает их. Наша задача: изменить это и дать людям информацию о новой протекторной защите».
судовые протекторы




Протекторы предназначены для защиты от коррозии объектов техники, эксплуатирующейся в
морской или речной воде: пассажирских судов и судов общегражданского
назначения, самоходных и несамоходных плавсредств, паромов, сухогрузных,
наливных, комбинированных судов специального назначения, земснарядов, отдельных корпусных конструкций и металлических сооружений, эксплуатирующихся в морской воде, а также нефте-газо-бензопроводов,портовых сооружений, причалов и т.д
Купить протекторную защиту можно наиболее удобным для Вас способом:
- Прислать запрос на электронную почту neva-dies@yandex.ru
- Оформить заказ
- Если Вы не нашли в Интернет-магазине продукцию, которая Вас интересует, свяжитесь со специалистом по тел. +7 812 336 43 34 или напишите нам
Протекторная защита (применение протектора):
Разновидностью катодной защиты является протекторная. При использовании протекторной защиты к защищаемому объекту подсоединяется металл с более электроотрицательным потенциалом. При этом идет разрушение не конструкции, а протектора. Со временем протектор корродирует и его необходимо заменять на новый.
Протекторная защита эффективна в случаях, когда между протектором и окружающей средой небольшое переходное сопротивление.
Каждый протектор имеет свой радиус защитного действия, который определяется максимально возможным расстоянием, на которое можно удалить протектор без потери защитного эффекта. Применяется протекторная защита чаще всего тогда, когда невозможно или трудно и дорого подвести к конструкции ток.
Аноды используются для защиты сооружений в нейтральных средах (морская или речная вода, воздух, почва и др.).
Для изготовления протекторов используют такие металлы: магний, цинк, железо, алюминий. Чистые металлы не выполняют в полной мере своих защитных функций, поэтому при изготовлении протекторов их дополнительно легируют.
Железные аноды изготавливаются из углеродистых сталей либо чистого железа.
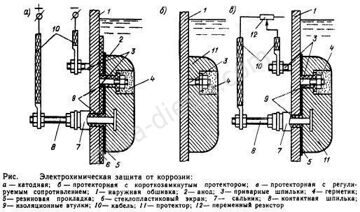
Полное прекращение коррозии возможно только в том случае, если на поверхности защищаемого металла не будет анодных участков. Искусственное превращение всей поверхности металла в катод достигается одним из способов электрохимической защиты: катодным или протекторным.
При катодной защите электропотенциал в морской воде изменяется наложением электрического тока от внешнего источника, для чего защищаемый объект соединяют с отрицательным полюсом источника постоянного тока, а его положительный полюс — со специальным электродом (анодом), погруженным в воду вблизи защищаемого объекта.Защита от коррозии этим способом обеспечивается установкой мощностью 3—5 кВт. Безопасность катодной защиты достигается применением источников тока с низким напряжением (до 24 В). В настоящее время применяются железокремниевые и платинотитановые аноды. Обычно достаточно установить 10— 12 анодов, чтобы обеспечить надежную защиту. Для равномерного распределения защитного тока аноды располагают равномерно по всему корпусу симметрично на оба борта.
Необходимо учитывать, что ток больше поглощается поверхностями, ближе расположенными к аноду. Поэтому вокруг анода делают экран — покрывают обшивку стеклопластиком.
Установленный на наружной обшивке анод должен быть хорошо изолирован от корпуса. В качестве
изолирующих прокладок обычно используют резину и армированные эпоксидные смолы.
Системы электрохимической защиты с наложенным током запрещается применять на танкерах.
Другой вид электрохимической защиты—протекторная защита или защита гальваническими анодами.
Ее особенность — отсутствие внешнего источника тока. Защитный ток в этом случае создают гальваническими элементами, которые образуются при установке на .корпус судна протекторов из металла с более низким потенциалом, чем у защищаемого. В такой гальванической паре корпус играет роль катода, а анодом являются протекторы. Благодаря этому в процессе электрохимической коррозии происходит разрушение протектора, а корпус судна коррозии не подвергается.
В качестве протекторов могут применяться металлы, которые имеют электродный потенциал ниже,
чем у стали. В настоящее время используются протекторы на магниевой и алюминиевой основе.
Протекторы в отличие от анодов должны иметь с корпусом судна электрический контакт. Обычно контакт осуществляется через приварные шпильки, с помощью которых протекторы крепят к обшивке. В некоторых случаях применяют отключаемые протекторы, которые имеют вводы внутрь судна и замыкаются на корпус через регулируемое сопротивление.
Простота выполнения и отсутствие эксплуатационных расходов обеспечивают широкие возможности
для применения протекторной защиты.
Однако на танкерах нельзя применять аноды из магниевых сплавов, а можно из алюминиевых.
Защита окрашенных балластных танков морских транспортных судов используется для уменьшения коррозионных разрушений на участках с местным повреждением лакокрасочных покрытий, на которых в отсутствие электрохимической защиты развивается точечная или язвенная коррозия.
Для неокрашенных поверхностей протекторная защита снижает общую скорость коррозии и предотвращает возникновение местных коррозионных разрушений.
{RANDOM_PARAGRAPH=401-800}
{RANDOM_SECTION=500-3000}





